新聞中心
基于自組裝肽的生物靈感材料有望解決生物醫(yī)學(xué)工程中的各種挑戰(zhàn)。雖然當(dāng)代的數(shù)據(jù)驅(qū)動(dòng)方法已經(jīng)發(fā)現(xiàn)了具有各種結(jié)構(gòu)和性質(zhì)的自組裝肽,但預(yù)測(cè)這些材料的功能仍然具有挑戰(zhàn)性。
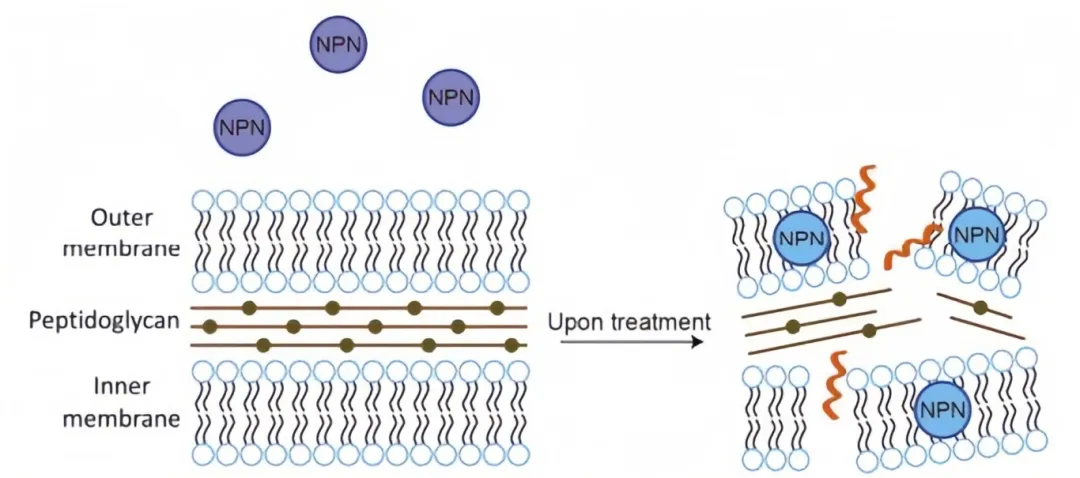
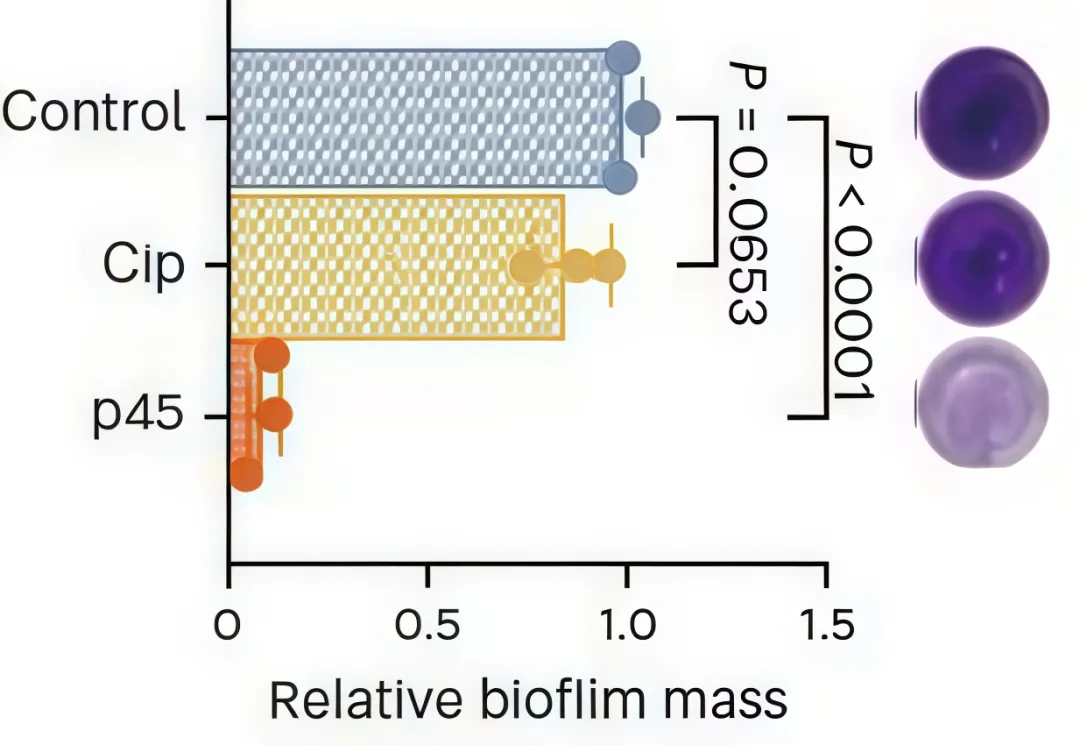
2025年3月14日,西湖大學(xué)理學(xué)院王懷民團(tuán)隊(duì)與生命科學(xué)學(xué)院黃晶團(tuán)隊(duì)合作,在Nature子刊Nature Materials上發(fā)表了題為“De novo design of self-assembling peptides with antimicrobial activity guided by deep learning” 的研究論文,該研究報(bào)告了一種基于深度學(xué)習(xí)的遷移學(xué)習(xí)模型——TransSAFP,從頭設(shè)計(jì)了具有抗菌活性的新型SAFP,以應(yīng)對(duì)當(dāng)前的細(xì)菌耐藥性問題。 該方法整合了非天然氨基酸用于增強(qiáng)的肽自組裝,并有效地預(yù)測(cè)了具有最小實(shí)驗(yàn)注釋的自組裝肽材料的功能活性。所設(shè)計(jì)的自組裝肽前導(dǎo)肽在小鼠體內(nèi)顯示出優(yōu)異的抗腸道細(xì)菌感染的治療效果。 此外,它表現(xiàn)出增強(qiáng)的生物膜根除能力,并且不會(huì)誘導(dǎo)獲得性耐藥性。機(jī)理研究表明,設(shè)計(jì)的SAFP p45能夠在細(xì)菌膜表面自組裝為納米纖維結(jié)構(gòu),通過物理方式破壞其膜結(jié)構(gòu),從而殺滅細(xì)菌,避免了傳統(tǒng)抗生素的靶點(diǎn)依賴性耐藥機(jī)制。 文章中利用細(xì)菌外膜透性實(shí)驗(yàn)(NPN法)來檢測(cè)細(xì)菌細(xì)胞膜的通透性變化,從而研究細(xì)菌的生理狀態(tài)和對(duì)外界環(huán)境的響應(yīng)。如果細(xì)胞外膜通透性增加,NPN進(jìn)入細(xì)胞內(nèi)部,熒光強(qiáng)度會(huì)增加?。 具體實(shí)驗(yàn)流程是: 鼠傷寒沙門氏菌在BHIB中培養(yǎng)至595nm處的光密度(OD595)為0.8,將細(xì)菌溶液以7000rpm(9860g)離心5分鐘,去除上清,用PBS重并洗滌三次。將50μl NPN溶液(40μM)加入96孔板中的50μl細(xì)菌溶液中,p45組加入100ul2X濃度的肽溶液,Control組加入100ulPBS。 信號(hào)檢測(cè)采用Varioskan LUX (Thermofisher),配備有熒光動(dòng)力學(xué)檢測(cè)功能,使用以下設(shè)置: 檢測(cè)溫度:37℃; 總測(cè)量時(shí)間:30min; 激發(fā)光波長(zhǎng):350nm; 發(fā)射光波長(zhǎng):420nm。 實(shí)驗(yàn)結(jié)果表明:p45中斷鼠傷寒沙門氏菌外膜的完整性,導(dǎo)致NPN熒光信號(hào)隨時(shí)間增加。 接著研究者做了生物膜形成和消除實(shí)驗(yàn)。具體實(shí)驗(yàn)流程是: 鼠傷寒沙門氏菌首先在平底96孔板中培養(yǎng)三天,每隔24h將96孔板中菌液倒出,用PBS洗滌三次以洗去未形成生物膜的菌體。用200μl的p45肽溶液浸泡4小時(shí)后用PBS洗滌以去除肽和浮游細(xì)菌。同時(shí),將經(jīng)PBS處理的生物膜設(shè)置為陰性對(duì)照,將空孔定義為陽性對(duì)照。加入100μL0.1%結(jié)晶紫溶液,靜止10min使生物膜充分染色。吸出結(jié)晶紫溶液,用PBS洗滌三次。向培養(yǎng)孔中加入100μL90%乙醇溶液,靜止10min充分溶解結(jié)晶紫。在595nm處測(cè)量每個(gè)孔所得的溶液吸光度。信號(hào)檢測(cè)采用Varioskan LUX (Thermofisher)。 相對(duì)生物膜質(zhì)量通過以下公式計(jì)算: 相對(duì)生物膜質(zhì)量=(OD?OD陽性對(duì)照)/(OD陰性對(duì)照?OD陽性對(duì)照) 實(shí)驗(yàn)結(jié)果表明:已建立的生物膜經(jīng)過p45處理4小時(shí)后幾乎完全消除,與對(duì)照組相比P<0.0001,而CIp環(huán)丙沙星組約90%的生物膜在治療后仍然存在。